 El número de implantes de asistencias circulatorias mecánicas para tratamiento de la insuficiencia cardiaca (IC) terminal está aumentando de forma exponencial en los países más desarrollados. Según el registro estadounidense INTERMACS1, se ha pasado de unas 100 intervenciones de este tipo en 2006 a más de 1.800 en 2011. En total, el registro incluye cerca de 7.000 pacientes con algún dispositivo de asistencia ventricular (VAD) de larga duración. La gran mayoría son VAD izquierdos de flujo continuo que, por su menor tamaño y mejores resultados, han sustituido a los de flujo pulsátil (figura 1). El objetivo más frecuente del implante de un VAD es permitir que los pacientes lleguen a un trasplante cardiaco (TxC), aunque cada vez es más frecuente implantar un VAD como terapia definitiva en pacientes no candidatos a TxC.
El número de implantes de asistencias circulatorias mecánicas para tratamiento de la insuficiencia cardiaca (IC) terminal está aumentando de forma exponencial en los países más desarrollados. Según el registro estadounidense INTERMACS1, se ha pasado de unas 100 intervenciones de este tipo en 2006 a más de 1.800 en 2011. En total, el registro incluye cerca de 7.000 pacientes con algún dispositivo de asistencia ventricular (VAD) de larga duración. La gran mayoría son VAD izquierdos de flujo continuo que, por su menor tamaño y mejores resultados, han sustituido a los de flujo pulsátil (figura 1). El objetivo más frecuente del implante de un VAD es permitir que los pacientes lleguen a un trasplante cardiaco (TxC), aunque cada vez es más frecuente implantar un VAD como terapia definitiva en pacientes no candidatos a TxC.
La supervivencia con estos dispositivos ha mejorado en los últimos años, y alcanza en la actualidad el 80% en el primer año y 70% a los dos años del implante. Los principales factores de riesgo de mortalidad postimplante son la situación crítica del paciente y la necesidad de implantar una asistencia biventricular, por lo que estos dispositivos se restringen en el caso de pacientes con shock cardiogénico establecido con daño de otros órganos y en pacientes con alto riesgo de fracaso del ventrículo derecho (VD) tras el implante del VAD.
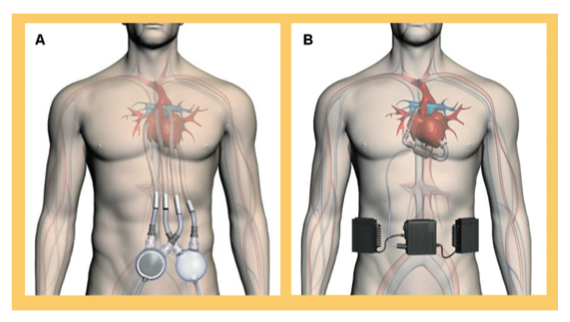
Figura 1: A) Dispositivo paracorpóreo de asistencia biventricular de flujo pulsátil. B) Dispositivo intracorpóreo de asistencia izquierda de flujo continuo.
La calidad de vida también mejora significativamente en la gran mayoría de receptores de un VAD, que habitualmente recuperan la autonomía para las actividades de la vida diaria, e incluso realizan actividad física moderada con asiduidad.
A pesar del alto nivel de desarrollo de nuestra medicina, en España solamente unas decenas de pacientes han sido tratados con VADs, debido a la relativa facilidad para conseguir donantes cardiacos hasta hace pocos años y al elevado coste económico que conllevan. En nuestro país son contados los hospitales con un programa estable de implante de estos dispositivos.
La Sociedad Internacional de Trasplante de Corazón y Pulmón (ISHLT) ha publicado recientemente unas guías sobre el manejo del soporte mecánico circulatorio de larga duración2, en un intento de consensuar los diferentes protocolos de cada hospital. Ante la escasez de evidencias sólidas procedentes de estudios correctamente diseñados, la mayoría de las recomendaciones están basadas en opiniones de expertos, y se agrupan en 5 apartados:
1) Selección de pacientes para implante de VADs. Los pacientes ideales son los que presentan disfunción sistólica del ventrículo izquierdo sin afectación importante del VD. La existencia de valvulopatías severas o shunts intracardiacos no corregibles, el infarto anterior reciente o la endocarditis infecciosa no controlada desaconsejan el implante de un VAD. Se consideran contraindicaciones la disfunción grave e irreversible de otros órganos, historia de incumplimiento del tratamiento, problemas psicosociales graves, adicción a tóxicos, coagulopatía o cualquier otra enfermedad que confiera una expectativa de vida menor de 2 años.
2) Cuidado del paciente previo al implante. Se debe intentar llegar a la cirugía en las mejores condiciones posibles de nutrición y de función de órganos. En algunos casos de shock con fracaso multiorgánico el uso de una asistencia mecánica circulatoria temporal tipo ECMO puede ‘rescatar’ al paciente para permitirle acceder al implante de un VAD más adelante.
3) Consideraciones intraoperatorias y cuidado postoperatorio inmediato. La técnica quirúrgica varía según el tipo de VAD y existe una curva de aprendizaje. El manejo cuidadoso perioperatorio del VD es fundamental, y para ello muchas veces es necesario utilizar inotrópicos y/o vasodilatadores pulmonares. La anticoagulación debe iniciarse en las primeras 24-48 h, cuando el paciente ya no presenta sangrado activo.
4) Recomendaciones para el periodo de hospitalización postoperatoria. La optimización del funcionamiento del VAD requiere ajustes del dispositivo guiados por ecocardiograma. Habitualmente en esta fase se reintroducen los fármacos utilizados en IC (betabloqueantes, IECAs, etc.) para control de la presión arterial y para facilitar una posible recuperación miocárdica en casos de cardiopatías potencialmente reversibles. Las complicaciones más frecuentes en este periodo (hemorragias, infecciones relacionadas con el dispositivo, disfunción del VAD, etc.) deben ser reconocidas y tratadas precozmente.
5) Cuidados del paciente ambulatorio a largo plazo. El paciente y las personas de su entorno deben estar capacitados para reconocer las posibles alarmas y problemas del dispositivo y solucionar situaciones de emergencia. Se les debe facilitar acceso al equipo médico experto y hacerles partícipes de algunos aspectos del autocuidado (control del INR, higiene de la zona de salida de la cánula o de la línea eléctrica según el tipo de VAD, etc.).
En resumen, cada vez es más frecuente el implante de asistencias mecánicas circulatorias de larga duración como tratamiento de la IC terminal. El éxito de la terapia, a corto plazo depende en gran medida de la selección de pacientes, la técnica quirúrgica y el tratamiento postoperatorio, y a largo plazo del compromiso del médico y el paciente en el cuidado excelente de su dispositivo y la salud personal.
Referencias
- Kirklin JK, et al. The INTERMACS annual report: Risk factor analysis from more than 6.000 mechanical circulatory support patients. J Heart Lung Transplant 2013;32:141-156.
- Feldman D, et al. The 2013 International Society for Heart and Lung Transplantation Guidelines for mechanical circulatory support: executive summary. J Heart Lung Transplant. 2013;32:157-87.





















































![La SEC te lleva a ACC24 Atlanta [POST]](images/portadaACC24-600.jpg#joomlaImage://local-images/portadaACC24-600.jpg?width=600&height=337)




















.png)






